Nguyên tử là đơn vị cơ bản của vật chất, và mỗi nguyên tử được đặc trưng bởi các yếu tố cơ bản như số proton, số neutron, và số electron. Những yếu tố này không chỉ xác định tính chất hóa học của nguyên tử mà còn ảnh hưởng đến cách mà nguyên tử tương tác với các nguyên tử khác. Trong bài viết này, chúng ta sẽ khám phá chi tiết về các yếu tố này và cách chúng đặc trưng cho một nguyên tử.
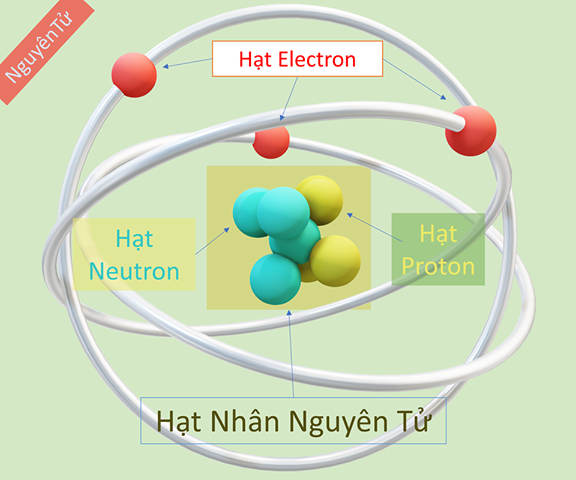
1. Số Proton và Điện Tích Hạt Nhân
Số proton trong hạt nhân của một nguyên tử được gọi là số nguyên tử (Z). Đây là yếu tố quan trọng nhất để xác định một nguyên tố hóa học. Mỗi nguyên tố có một số nguyên tử duy nhất. Ví dụ, tất cả các nguyên tử của nguyên tố carbon đều có 6 proton trong hạt nhân. Số proton cũng quyết định điện tích hạt nhân, vì mỗi proton mang một điện tích dương.
Điện tích hạt nhân ảnh hưởng đến lực hút giữa hạt nhân và các electron, từ đó ảnh hưởng đến kích thước của nguyên tử và năng lượng ion hóa. Năng lượng ion hóa là năng lượng cần thiết để loại bỏ một electron khỏi nguyên tử. Nguyên tử có điện tích hạt nhân lớn thường có năng lượng ion hóa cao hơn vì lực hút giữa hạt nhân và electron mạnh hơn.
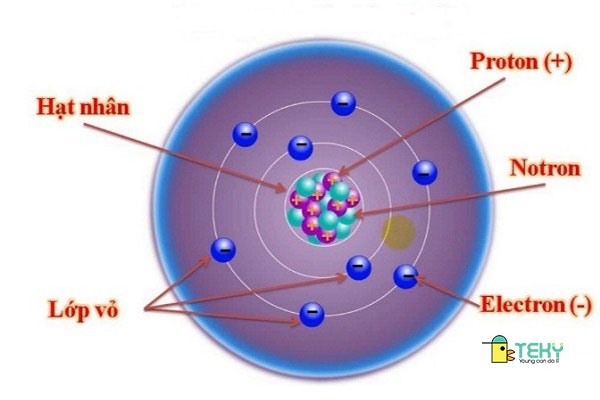
2. Số Neutron và Số Khối
Số neutron trong hạt nhân của một nguyên tử không ảnh hưởng đến tính chất hóa học của nguyên tố, nhưng nó ảnh hưởng đến khối lượng và tính ổn định của hạt nhân. Số khối (A) của một nguyên tử là tổng số proton và neutron trong hạt nhân. Ví dụ, một nguyên tử carbon-12 có 6 proton và 6 neutron, do đó số khối của nó là 12.
Các đồng vị của một nguyên tố có cùng số proton nhưng khác số neutron. Ví dụ, carbon có hai đồng vị phổ biến là carbon-12 và carbon-14. Mặc dù chúng có cùng số proton, nhưng số neutron khác nhau làm cho chúng có khối lượng khác nhau và tính chất vật lý khác nhau. Carbon-14, với 8 neutron, là một đồng vị phóng xạ và được sử dụng trong phương pháp định tuổi bằng carbon.
3. Số Electron và Cấu Trúc Electron
Số electron trong một nguyên tử thường bằng số proton, làm cho nguyên tử trung hòa về điện. Các electron quay quanh hạt nhân trong các lớp vỏ electron. Cấu trúc của các lớp vỏ này quyết định cách mà nguyên tử tương tác với các nguyên tử khác và hình thành liên kết hóa học.
Các electron trong lớp vỏ ngoài cùng, gọi là electron hóa trị, đóng vai trò quan trọng trong các phản ứng hóa học. Số electron hóa trị quyết định tính chất hóa học của nguyên tố. Ví dụ, các nguyên tố trong nhóm 1 của bảng tuần hoàn, như natri và kali, có một electron hóa trị và dễ dàng mất electron này để tạo thành ion dương.
4. Ứng Dụng Thực Tiễn và Nghiên Cứu
Hiểu rõ về cấu trúc nguyên tử và các yếu tố đặc trưng của nó có nhiều ứng dụng thực tiễn trong khoa học và công nghệ. Trong y học, các đồng vị phóng xạ được sử dụng trong chẩn đoán và điều trị bệnh. Trong công nghiệp, các nguyên tố hiếm và các hợp chất của chúng được sử dụng trong sản xuất điện tử và vật liệu tiên tiến.
Nghiên cứu về nguyên tử cũng giúp chúng ta hiểu rõ hơn về các hiện tượng tự nhiên và phát triển các công nghệ mới. Ví dụ, nghiên cứu về cấu trúc nguyên tử và các phản ứng hạt nhân đã dẫn đến sự phát triển của năng lượng hạt nhân và các ứng dụng của nó trong sản xuất điện và vũ khí.
5. Kết Luận
Một nguyên tử được đặc trưng cơ bản bằng số proton, số neutron, và số electron. Những yếu tố này không chỉ xác định tính chất hóa học của nguyên tử mà còn ảnh hưởng đến cách mà nguyên tử tương tác với các nguyên tử khác. Hiểu rõ về cấu trúc nguyên tử và các yếu tố đặc trưng của nó là nền tảng của nhiều lĩnh vực khoa học và công nghệ.
Để tìm hiểu thêm về các khái niệm này và các ứng dụng của chúng, bạn có thể truy cập trang web Học Trực Tuyến Toliha tại toliha.vn. Trang web cung cấp nhiều tài liệu học tập và bài giảng trực tuyến giúp bạn nắm vững kiến thức về hóa học và nhiều lĩnh vực khác.
Hy vọng bài viết này đã giúp bạn hiểu rõ hơn về cách mà một nguyên tử được đặc trưng cơ bản bằng các yếu tố như số proton, số neutron, và số electron. Nếu bạn có bất kỳ câu hỏi nào hoặc cần thêm thông tin, đừng ngần ngại liên hệ với chúng tôi qua trang web Toliha.
